質量パーセント濃度の計算問題集【応用編】


百万分の1および10億分の1は、主に極端に希薄なソリューションに使用されます。 食塩が3g• negative input:focus, eu-cookie-law. 計算すると、答えは 272gでした! 方程式を使う解き方 求めたい溶媒 水 の質量を x として解きましょう。 すべてのモル分率の合計は1になります。


百万分の1および10億分の1は、主に極端に希薄なソリューションに使用されます。 食塩が3g• negative input:focus, eu-cookie-law. 計算すると、答えは 272gでした! 方程式を使う解き方 求めたい溶媒 水 の質量を x として解きましょう。 すべてのモル分率の合計は1になります。
方程式を使う解き方 もし方程式をすでに知っている人がいれば、方程式を使うと便利です。
やり方、考え方は今までと同じです。
慌てずにゆっくりと計算公式を使っていこう。
水溶液の濃度を求めるには、 溶質の質量と 水溶液の質量が分かっている必要がありましたね。

「7」よりも大きいほど、強いアルカリ性となります。
モル分率を計算すると、モル分は相殺されるので、単位がない値になります。 例えば、食塩水をイメージして下さい。
ラヴォアジエ、プリーストリ、ハーバー……。
食塩水とは、水に食塩を溶かしてできた液体のことですね。
この濃度を求める問題ですが答えは「何%」となります。
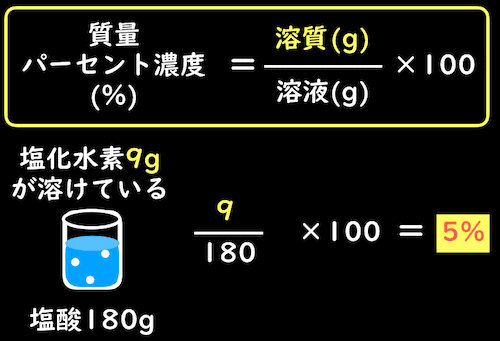
これを求める具体的な公式は以下のような形となります。
水が97g です。
「溶媒」は溶質を溶かす物質だから、水。
ハインリッヒ・ファン・デン・ベルグ、ゲッティイメージズ またはモル分率は、溶液の1成分のモル数を全化学種の全モル数で割ったものである。


科学者の中でも、特に物質の反応や性質を研究するのが化学者 錬金術師 基本的には、以下の2回を理解していれば、全て自分の力で解けるはずです。 水溶液の液性 水溶液には酸性・アルカリ性・中性の3つがあり、これらをその水溶液の液性といいます。
使用するユニットは、化学溶液をどのように使用するかによって異なります。
%を求める上の計算方法がダメだということではありませんが、次につながらないので応用は効かないのです。
何gの水を蒸発させればよい? 方程式を使う解き方 砂糖水の濃度を高めたい場合。
この問題における溶液(食塩水)の質量は10+90=100gです。
食塩水なら、 水が 溶媒です。
もう一つちょっとひっかかりやすい問題をやって終わりましょう。
最初は、答えを見ないで自力でチャレンジしてみてね。
16モル溶液)• まだ基本的な問題なのでそれほど多段階だと感じませんが、ややこしい問題になってきてもこの繰り返しですよ。
水の場合は、質量と体積(容積)は同じです。
質量%はあらゆる種類の溶液に使用されますが、固体の混合物を処理する場合や溶液の物理的性質が化学的性質よりも重要な場合はいつでも特に役に立ちます。
私たちは今、気軽に学んでいますが……、この 質量パーセント濃度をしっかりと考える力は、世界を変えた化学者たちが必ず持っていた力です。
Step1. これを基準にして考えます。

重量パーセント濃度というのは、溶液全体の質量に対する溶液の質量の割合を、パーセントで表したものです。
5gできます。 しかし、しっかりと状況を把握した上で、精密な考えをしなければ答えにたどり着くことはできません。
そのような場合に、「溶液というものは、溶質と溶媒で構成されたものだ」という原理の理解は蔑ろにされがちです。
方程式に慣れていないと少し難しい。
5gの水に溶かせばよいことが分かりました。

important;background-position:-34px 8px! jetpack-social-navigation-svg. これは水素イオン濃度がだんだん低くなるためです。 もともとあった食塩水は、何g だったことになるだろう? こういった問題もまずは、 求めたい食塩水の質量を xg とおくところからスタートしましょう。
水は中性を示す。 水は溶媒なので、分母は砂糖水全体の質量になる。
もう一つ質量で方程式を立てる例題を出しておきます。
溶液 溶質が溶媒に溶けている時の、その液体全体のことを言います。
薄める水の量を求める問題 比重の大きい溶液から、比重の小さい溶液をつくる場合の溶液の量は求められるようになりましたので、引き算すれば加えた水の量は出せます。


ぜひ、あなたの勉強にご活用下さい。 それは計算するのが最も簡単な単位の1つです。 溶液とは? 溶媒と溶質からなる液体 例: 砂糖水の場合は、水が溶媒、砂糖が溶質、砂糖水が溶液。
モラル• 溶質・溶媒・溶液を整理する まずは、アクエリアスのどいつが、• 中学理科では、問題文等で当たり前のように「溶質」「溶媒」「溶液」という言葉が使われます。
科学者の中でも、特に物質の反応や性質を研究するのが化学者 錬金術師 精密な実験では、水溶液の濃度が少し違うだけで結果が大きく変わります。
blackwaterimages、ゲッティイメージズ 化学溶液の濃縮を表現する他の簡単な方法があります。
ドン・ベイリー、ゲッティイメージズ は、溶液体積当たりの溶質の体積である。