テセントリクとアバスチン、切除不能な肝細胞がんに対する併用療法で承認取得

冊子の各副作用項目に記載している「程度の目安」のグレードは、医療者が用いている「有害事象共通用語規準 Common Terminology Criteria for Adverse Events 日本語訳JCOG版」や文献などを参考に、患者さんに分かりやすい表現にして用いています。 Grade 3以上の場合 本剤を直ちに中止する。
11

冊子の各副作用項目に記載している「程度の目安」のグレードは、医療者が用いている「有害事象共通用語規準 Common Terminology Criteria for Adverse Events 日本語訳JCOG版」や文献などを参考に、患者さんに分かりやすい表現にして用いています。 Grade 3以上の場合 本剤を直ちに中止する。
11化学療法未治療のPD-L1陽性の切除不能な進行・再発の非小細胞肺癌 通常、成人にはアテゾリズマブ(遺伝子組換え)として1回1200mgを60分かけて3週間間隔で点滴静注する。
臨床成績」の項の内容を熟知し、十分な経験を有する病理医又は検査施設における検査により、PD-L1の発現が確認された患者に投与すること。
高血圧、蛋白尿、出血など注意を要する副作用はあるもののそれもリスクに応じた対処がされていれば多くの場合問題ないでしょう。
Grade 4又は再発性の膵炎 本剤を中止する。

【発表】 2018年6月4日 【試験名】 IMpower150(Phase 3)〔〕 【原著】 [PMID: ] 【内部リンク】• 血管やリンパ管などに残存した可能性のあるがん細胞が再発することを予防する目的で行われる治療方法です。
16患者さんからは「具体的に書いてあり、安心感につながった」などの声をいただいています。
冊子は、下記の「 」の更新日(閲覧・印刷時に各冊子タイトル下に記載のある年月日)時点の情報で作成しており、治療や薬の情報、制度などは変更される場合があります。
冊子の種類は、順次拡大し掲載予定です。
現在までに作成したがん薬物療法(抗がん剤治療)の冊子を掲載しています。
2次治療 1次治療の効果が得られなくなった、または継続できない副作用が生じた際、2番目に行うがん薬物療法(抗がん剤治療)です。
例えば、主な副作用の現れやすい時期、頻度が一覧表になっています。
このようにこの2剤併用療法は初めてネクサバールに対してOSで優位性を示したレジメンですので、まず有効性面で文句なしと言えるのです。
なお、初回投与の忍容性が良好であれば、2回目以降の投与時間は30分間まで短縮できる。
病気の種類・使用する薬の組み合わせ別に、患者さんに知っておいてほしい内容を1冊にまとめました。 このような患者にテセントリクを投与すると、間質性肺疾患の症状があらわれたり、その症状が悪化する恐れがあります。
・症候性の甲状腺機能低下症 ・症候性の甲状腺機能亢進症、又は甲状腺刺激ホルモン値0. 肝予備能についてはChild-Pugh score 癌のステージについては各国ガイドラインがありますが、Barcelona Clinic Liver Cancer(BCLC)stagingを用いることも多いです。
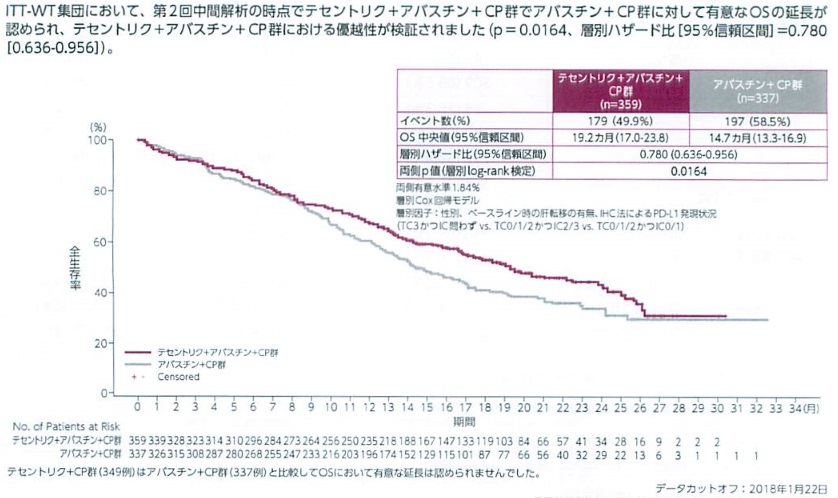
オンコロジー領域の治療薬を評価する上ではやはりなんと言ってもOSですよね。
58 死亡リスクを42%軽減 です。

肝機能障害(切除不能な肝細胞癌を除く) Grade 2(AST若しくはALTが基準値上限の3倍超かつ5倍以下又は総ビリルビンが基準値上限の1. 非扁平上皮がんの人が初めての治療を考える場合、「化学療法(+)+」に「」の上乗せを選択することで、生存期間および無増悪生存期間の延長が期待できる。
19これまでテセントリクとアバスチンの併用は他のがん種を見る限りロシュの戦略ミスだな、と思っていましたが、これに関しては恐れ入りました。
そもそも免疫チェックポイント阻害薬は従来の抗がん剤と比べると副作用はマイルドです。
眼障害 Grade 2の場合 Grade 1以下に回復するまで、本剤を休薬する。
作成にあたっては、データインデックス株式会社の協力を得ながら進め、2017年より医師・看護師・薬剤師がこの冊子を用いて患者さんに説明を行っています。


HCC治療への貢献を目指し、引き続き迅速な適正使用情報の提供に努めてまいります」と語っている。 副腎機能障害 副腎機能不全(0. がん薬物療法(抗がん剤治療)は、たくさんの種類があり、「治療法」が同じでも適応基準が異なる場合があります。
1112週間を超える休薬後もGrade 1以下まで回復しない場合は、本剤を中止する。
Grade 2の場合 投与を中断し、軽快後に投与速度を50%に減速し再開する。
副作用 程度 処置 間質性肺疾患等の呼吸器障害 Grade 2の場合 Grade 1以下に回復するまで、本剤を休薬する。
集計結果を公表することがありますが、個人が特定される情報を公表することはありません。

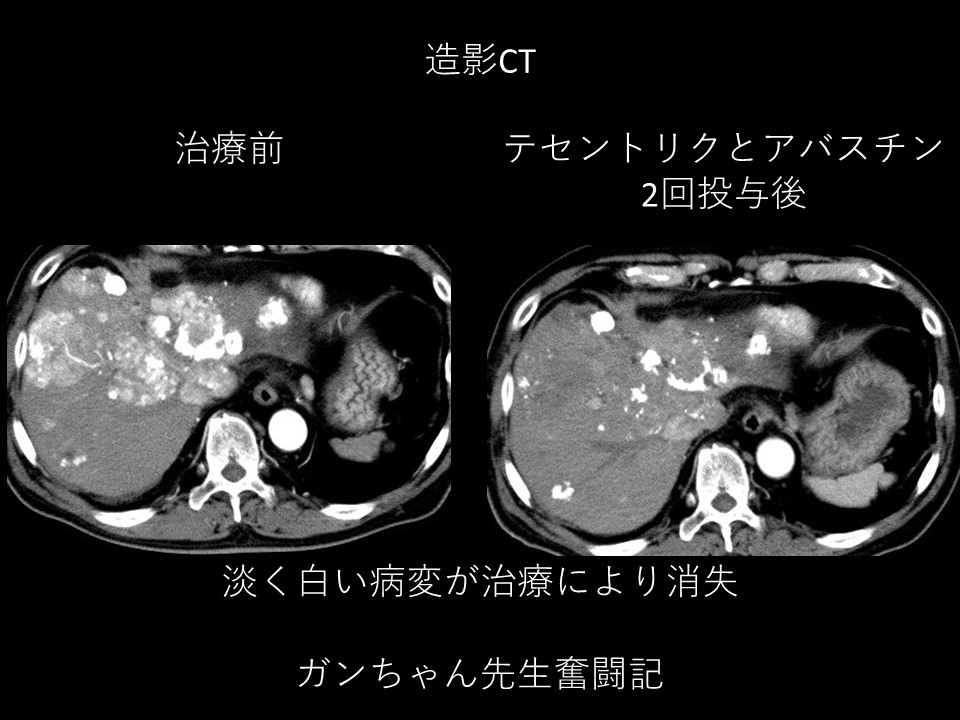
本試験成績は、2020年5月14日にに掲載されました。 投与間隔は3週間以上とする。
また、投与量や投与間隔はどのがんに対して使用するかによって異なります。 HCCは肝臓がんの9割以上を占め、 不良かつ全身薬物療法の選択肢は限定的であるため1年生存率は50%以下である。
上の図でも罹患数は5位に入っていないのに死亡数は5位になっていますので、そういうことですよね。
12週間を超える休薬後もGrade 1以下まで回復しない場合は、本剤を中止する。
大腸炎、重度の下痢 大腸炎(1. 9ヶ月)と、テセントリク+アバスチン併用群で死亡(OS)のリスクを34%( :0. テセントリクを投与するにあたり起こる可能性がある重大な副作用について、下記の表にまとめています。
テセントリクとアバスチンが投与された329例中276例(83. 2%という数字が表すように予後不良 のがんと言えます。
ご利用にあたっての注意事項 冊子は、静岡がんセンターの医療者が作成し、正確な内容となるよう努力していますが、診断、治療、その他医学的な情報が、常に最新かつすべての人に当てはまるとは限りません。
ほんとに肝細胞がんにはこの組み合わせが良かったんだろうな、としみじみと感じています。
肝細胞癌の治療は、肝予備能 肝臓の働き 、癌の進行度等で決定されます。