血液 脳 関門 通過。 血液脳関門/BBB/
血液脳関門の通過技術を開発 JCRファーマが治療薬の開発に着手: J
脳微小血管内皮にクローディン5を薬剤誘導性にノックダウンできるマウスを作成し、成熟マウスでクローディン5の持続的なノックダウンを行った場合、マウスはや、、プレパルス・インヒビション(prepulse inhibition、PPI)の低下を示した。 個人的には、一年でも早く有効なアルツハイマー治療薬が出てきてほしいと思ってるので、「JR-141」のフェイズ1の結果に最も期待しています。 その障壁のことを血液脳関門と呼ぶ。
18
血液から脳実質内へのアクセスは血液脳関門の他に(BCSFB)がある。
さらにクローディン5は蛍光共鳴エネルギー移動(FRET、またはフェルスター共鳴エネルギー移動)を用いてクローディンファミリーのシス相互作用とトランス相互作用を評価した検討ではクローディン5同士は非常に強いシス相互作用とトランス相互作用が認められた。
2017 Jan 3;114 1 :E75-E84,• 2013 Jan 10;10 1 :5,• 周皮細胞(ペリサイト) 内皮細胞に接してすぐ外側の1枚の基底膜を介して位置する不整形、多角形の細胞である。
サイズ選択性の乏しい物理的な方法 [ ] サイズ選択性の乏しい物理的な方法にはによるもの、収束超音波(focused ultrasound)を用いるもの、を用いるものがある。
血液脳関門を誤解してました(*_*)
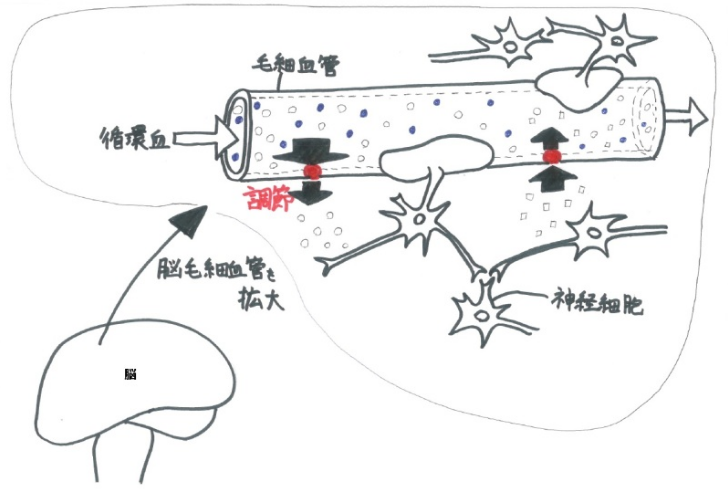
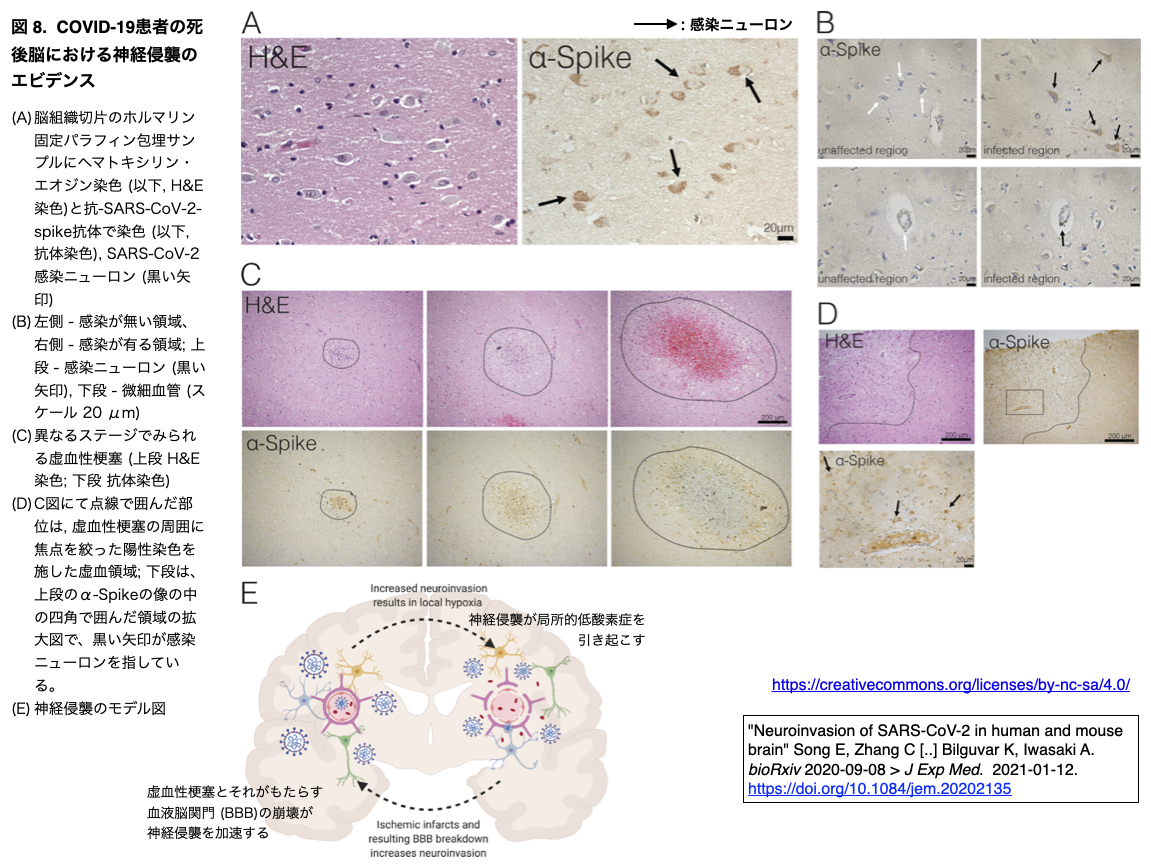
そのためには血中に投与された薬物を脳微小血管内皮細胞近傍に標的化し、かつ血液脳関門の透過性を亢進させる必要がある。
7
しかし、そのゲートがどこにあるのか、またどのように形成されるのかなど、実体は不明でした。 血液脳関門のin vitroモデルはトランスウェル transwell を使用した培養が一般的である。
インスリンは脳では合成されないがRMTの機序で血液脳関門を通過し脳で作用する。
J Comp Neurol. 血液脳関門とは? 血液脳関門 Blood Brain Barrier : BBB は1913年に初めて報告されました。
2016年に販売された製品のため、2017年3月期の販売金額としては7億程度ですが、会社は今後飛躍的に伸びていく予想を立てています。
JCRファーマの株価はもっと高くていいだろ?血液脳関門通過技術に期待

だが、アンチセンス核酸薬が血液脳関門を通過できる量はあまりにも少なく、これまで患部の遺伝子に作用させることが難しかった。
1
や膿瘍、またそれらに付随する炎症反応は血液脳関門を部分的に破壊する。 炎症細胞の細胞浸潤は内皮細胞の胞体を突き抜けるtranscellular migrationでありタイトジャンクションの制御する内皮細胞間ではない。
たとえば、血液のpHが変化した場合、この変動が脳に伝わってはなりません。
低分子の有機化合物は、薬物排出トランスポーターとしてよく知られている ABC ATP Binding Cassette トランスポーターで脳実質から排出することによって、神経組織を保護している。
多発性硬化症 注4 の動物モデルである実験的自己免疫性脳脊髄炎 EAE 注5 をマウスに発症させ、EAEの原因となる自己反応性T細胞を正常マウスの血管内に移入すると、正常マウスの中枢神経系にEAEが誘導されます。
血液脳関門を誤解してました(*_*)
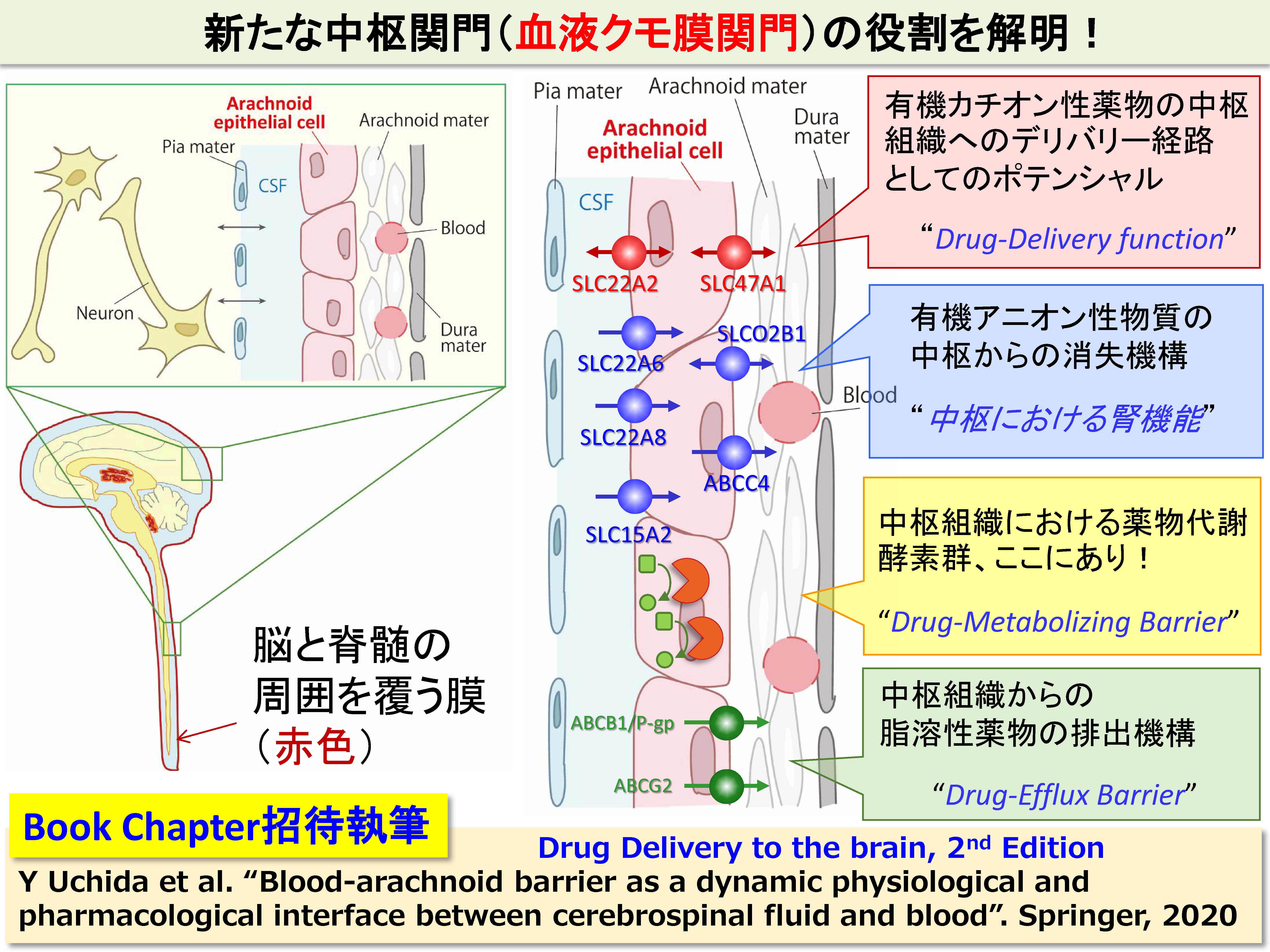
製品の革新性から言っても、臨床現場で安全性や有効性が周知されてこれば、大きな収益の柱に育っていくでしょう。 Contribution of carrier-mediated transport systems to the blood-brain barrier as a supporting and protecting interface for the brain; importance for CNS drug discovery and development. しかしペプチドのクローディン5選択性は乏しいと考えられる。
6
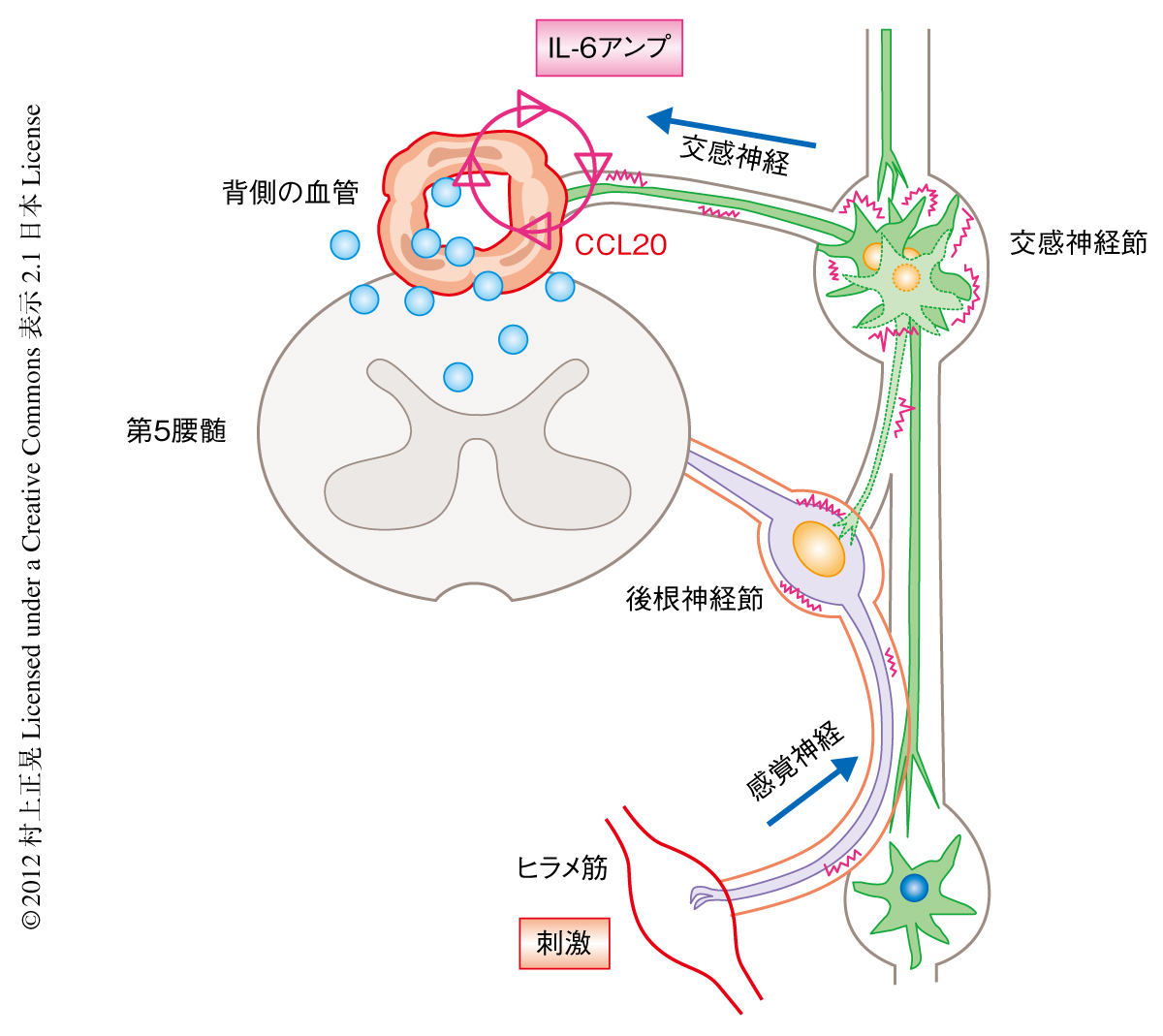
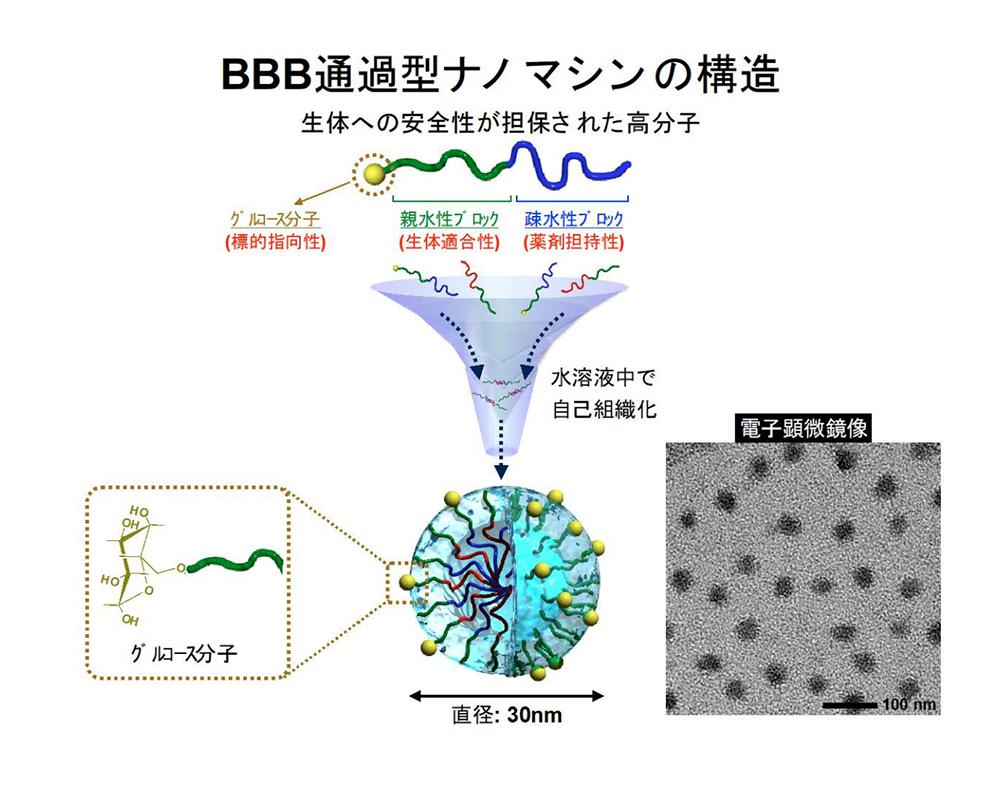
収束超音波と同様にマンニトールもタイトジャンクション構成分子のリン酸化状態を変更することで構成蛋白質を分解させる。 高分子でできた直径約30ナノの粒子の表面にグルコースを結合させて、空腹もマウスに投与した。
だが、ニコチンがどうやって血液脳関門を通ることができるのか、そのメカニズムはよくわかっていない。
同様の用途としてインシュリン受容体も利用されます。
5種の異なるリガンドで修飾したで脳微小血管内皮細胞への取り込み効率を比較したin vitro実験では全てが細胞内に取り込まれたがマウスに静脈注射したin vivoの実験ではそのうち1種類しか脳標的化作用を示さなかったという報告がある。
血液脳関門を通過できない物質 できる物質とは?

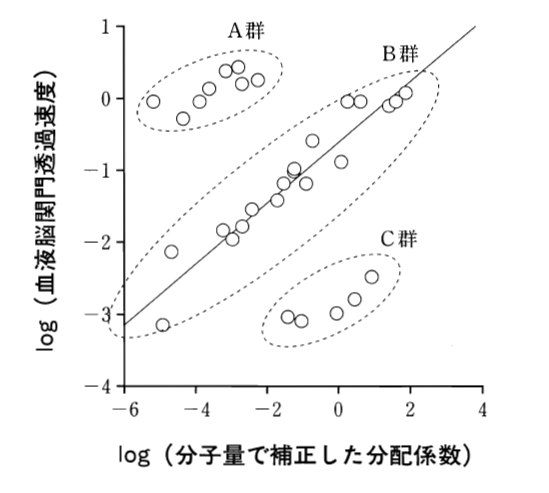
BNBを構成する微小血管内皮細胞と同様に4つの特徴が知られている。
20
このノックダウンによる低分子の透過亢進は3日程度持続し、1週間以内にバリアー機能が回復する。 それらの細胞が、血管内から中枢神経系に入り込む部位を特定するために、切削器具のマクロトームを用いて脊髄を薄くスライスし、蛍光顕微鏡で解析しました。
オクルディンはタイトジャンクションを構成でき、生存可能である。
一方、など脂溶性の低い物質は脳血管が透過することができない。
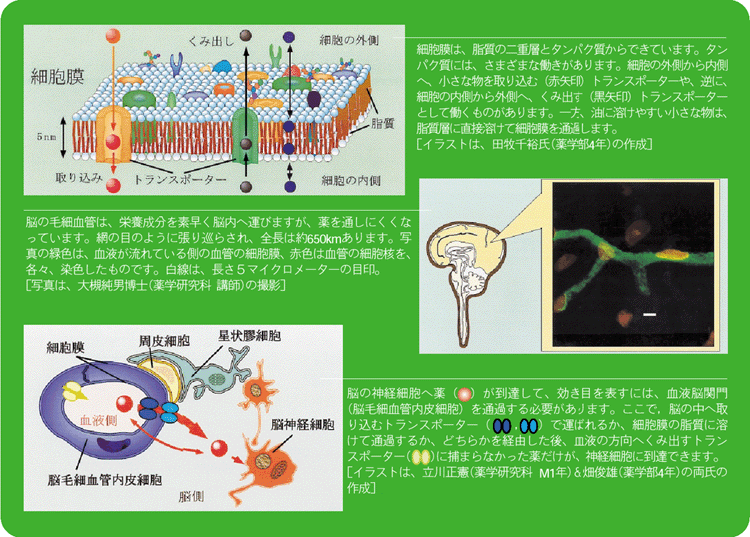
血液脳関門と物質の脳内への移行 すべての物質は、脳に入る前に、 血液脳関門(BBB:blood brain barrier)という関所を通過しなくてはいけません。
血液脳関門を通過できない物質 できる物質とは?
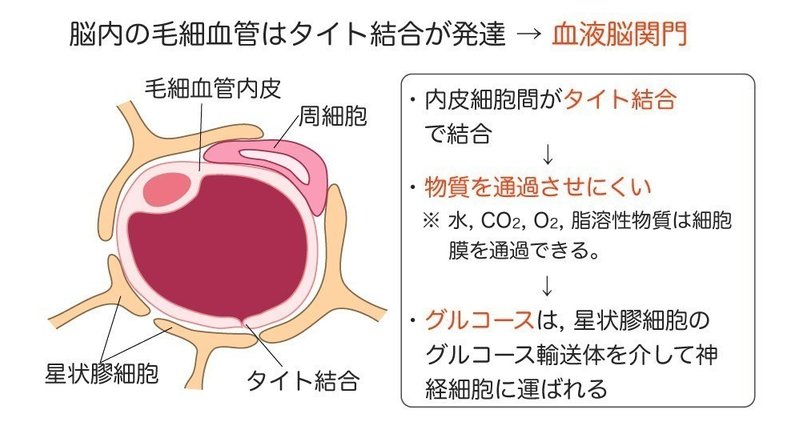
実際に物質が脳の中に移行するかを調べなければ、本当に移行するかはわからないです。
抗体以外にクローディン5の細胞外領域に結合するペプチドも知られている。 もともと血中に存在する内因性トランスフェリンが過剰濃度で存在するためトランスフェリンをリガンドとして活用するのは難しいと考えられた。
Pardridgeらによって達成された。
脳のバリアをどう突破するか このように脳関門や網膜関門などの身体の関門は、外部からの異物の侵入を防ぐバリアでもあるが、同時に患部へ薬を運び入れるのを阻害する厄介な機構だ。
Kempermann, G. も含めれば1 も報告がある。
血液脳関門/BBB/
 薬物の脳への移行 1 (1).png?height=253&width=400)
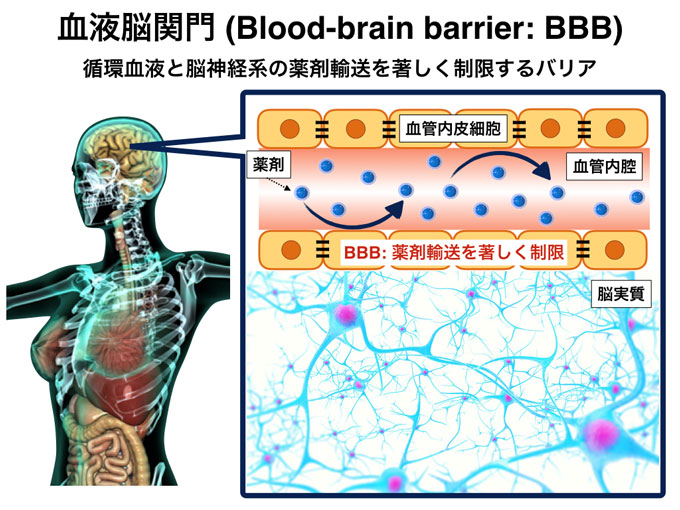
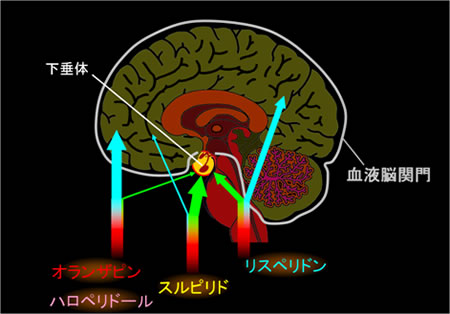
によれば、脳内の毛細血管の細胞が接する部分の密着結合(血液脳関門)に作用するアンギュビンディン1というタンパク質の断片をマウスに静脈注射し、その後、アンチセンス核酸薬を静脈注射したところ、アンチセンス核酸薬が従来より大量に脳や脊髄に到達し、ターゲットとなる遺伝子の発現が約40%抑制されたという。 血液脳関門が脳神経細胞の活動に欠かせないアミノ酸などを通すことに着目。 一方で吸着性トランスサイトーシスは負電荷である細胞表面に吸着するカチオン性のタンパク質、アルギニン等のカチオン性アミノ酸が豊富にある膜透過性ペプチド CPPs があります。
8
恒常的に1kDa以下の低分子が脳内に流入し続けると脳内環境が破綻し致命的な脳内炎症が生じることが示唆されている。 特にクローディン5の持続的なノックダウンでマウスが死亡することから、恒常的に1kDa以下の低分子が脳内に流入し続けると脳内環境が破綻し致命的な脳内炎症が生じることが示唆される。
JCR 血液脳関門通過型ハンター症候群治療酵素製剤「JR

血液液バリアの障害は、あらゆる形態の髄膜炎(髄膜炎)で発生します。
1
, 560, 167-174 1991 []• もちろん、投資は現物余剰資金、そして自己責任を忘れずに。











 薬物の脳への移行 1 (1).png?height=253&width=400)

