化学I 基礎理解

でも普通の酸と金属としての反応は一応考えられるわけですから少なくともそのことについては書いて欲しいです。 一酸化窒素は、水に不溶であるため、水上置換によって捕集します。 炎はナトリウムの炎色反応を示し黄色になる。
19

でも普通の酸と金属としての反応は一応考えられるわけですから少なくともそのことについては書いて欲しいです。 一酸化窒素は、水に不溶であるため、水上置換によって捕集します。 炎はナトリウムの炎色反応を示し黄色になる。
19教科書には酸化作用により鉄の表面に丈夫な酸化膜が出来て反応が進まなくなると載っています。 苦労してやった結果が穴にはまるのです。
こんにちはデビッド、 上限を超える割合であるため、製品に影響を与える可能性はほとんどありません. ここの「この式の左辺のH+をHNO3に、右辺のCu2+をCu(NO3)2に置き換える。
化学反応式の両辺で酸化数の総和は変わらないから、 生成したNO2とO2の比は4:1になる。
. 多くの異なる方法が表示されますが、標準化された方法に関連付けられているものはありません. これらの反応は,それぞれ二酸化窒素や一酸化窒素を実験室で得る方法として用いられています。
ATKINS, INORGANIC CHEMISTRY Third Edition, 1999. その化学反応式は次の通り。
また、未定係数法の解き方もよろしければ教えてください。
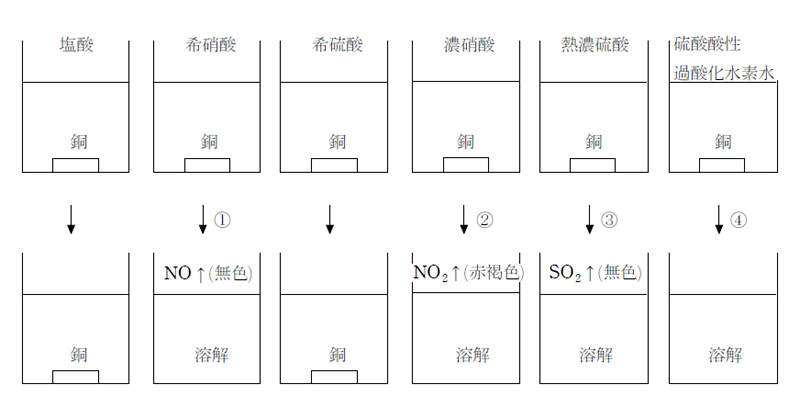
バッチテストに合格する以外に、パッシベーションされたパーツのサンプルを見て、それらがエンドグレインピットや粒間攻撃の影響を受けていないことを確認できます(何か良い兆候が発生している). また,硝酸はいろいろな金属と反応しますが,濃硝酸はアルミニウム,鉄,ニッケルなどとは反応しません。
普通に考えると「水素を出して溶けて2+のイオンになり、その後3+に酸化される」となります。
監査人から、メソッドの入手先が尋ねられました。 塩酸や硫酸には水素を発生して溶けます。
今回はここまでにしましょう。
山崎一雄他 『無機溶液化学』 南江堂、1968年• 県や市のホームページに毒物及び劇物取締法に関して記載されていますので、そちらに問い合わせてみてはいかがでしょうか。
. 詳しくは以下のサイトをご覧ください。
一酸化炭素の燃焼(1) 一酸化炭素と酸素をチューブに入れ,点火して反応させる。 自分ではこう考えた、ここが分からないということを書くべきです。
一酸化窒素 の算出を促すと、脳卒中や心筋梗塞の防止につながることもいわれ、関連の研究が進んでいるそうです。
皆さんこんにちは、 私達は最近不動態化ラインを始めました、そして私は25%の硝酸塩と2%の重クロム酸ナトリウムの鉄分を決定するための手順を探していました. と書いてあったのですが、これがなんで4:1になるのか分りません。
硝酸には酸化に関与したものと、中和(塩の形成)に関与したものがあると言うことになります。

次に、冷まし、DI H2Oで100 ml程度に希釈し、フェロイン指示薬を追加し、標準の重クロム酸ナトリウム溶液で赤い終点まで滴定します。 なお、の生態系において嫌気性菌のは困難であり、中に硝酸が分解されないまま溜まっていくので、高となる以前の適度な水換えが必要となる。 メソッドが導入されてからここで作業を始めるまで、私にはわかりません。
しかし、審査員は実際的な人ではありません。
これを未定係数法と呼びます(参考URL)。
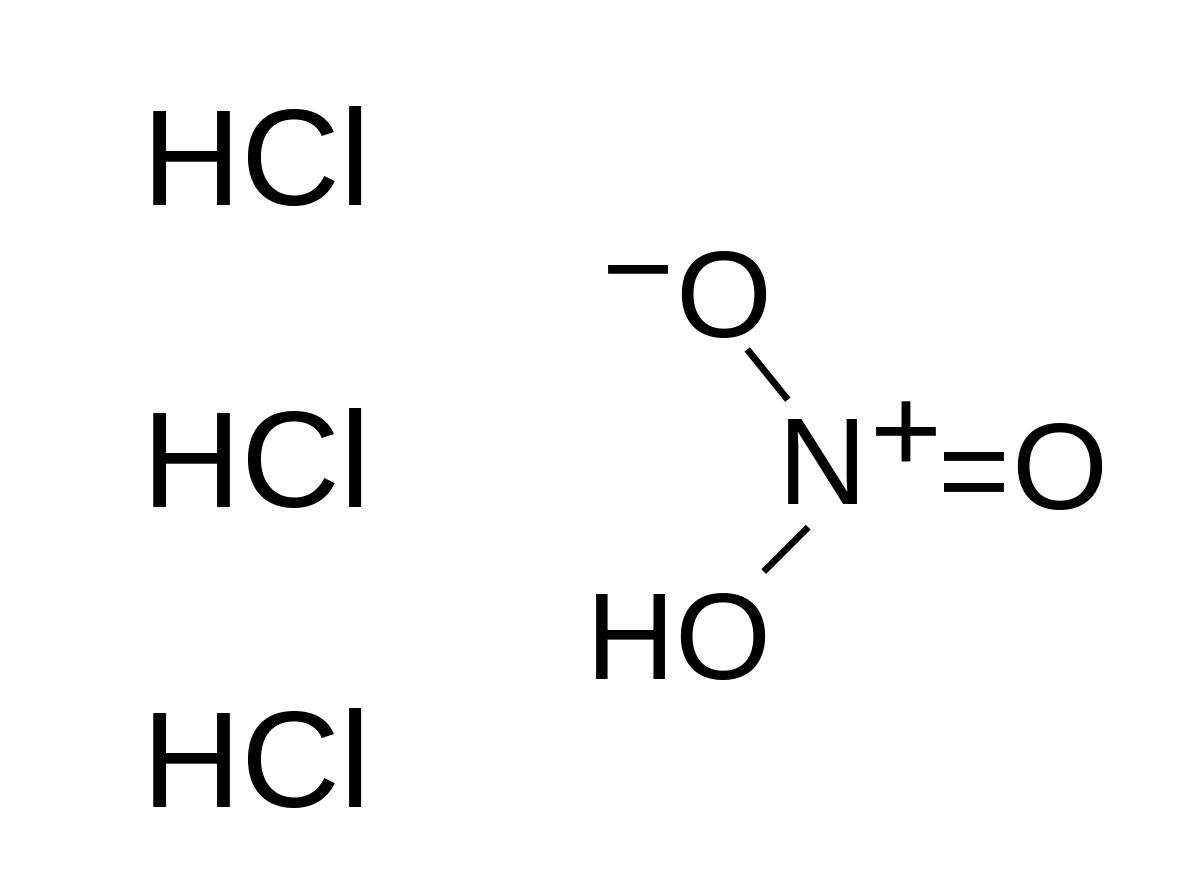
硝酸は単体の名称ではなく、 水H 2Oに二酸化窒素NO 2という気体が溶け込んでできる混合物のことを指します。
. 鉄イオンには2+のものと3+のものがあります。
提示されたすべての情報は一般的な参照用であり、専門家の意見や著者の雇用主の方針を表すものではありません. 二酸化炭素に浮かぶシャボン玉 シャボン玉の中の空気の密度は二酸化炭素の密度より小さいので,シャボン玉は落ちない。
本当は、 希硫酸 電離度が大きい(水素イオン濃度が大きい) 濃硫酸 電離度が小さい(水素イオン濃度が小さい) と書きたかったのだと思いますが、その本の記述は、強酸・弱酸と、濃度による電離度の違いを混同しています。
鉄と硝酸の反応はけっこう難しいです。
例として、銅と希硝酸の反応式書いてみます。


ページ (あなたはスレッドの最後のページにいます) 議論は2011年に始まりましたが、2019年まで続きました Q. 私は手紙40281からこの手順を見つけました: 1-既知の重量をバスから取得W(15-25 gm). 1 2 3 3 フェノールは 1 性で,水酸化ナトリウム水溶液と反応して 2 を生じ,水に溶ける。 約5 mLのDIが入った清潔なビーカーに5 mLのバスのサンプルを置きます. 課題となったのは白金触媒に関してですが、自動車排ガス用の使用済み白金触媒を自動車解体業者から入手して使用しています。 そうでなければ「式(1)の係数を求めよ」という問と変わらないからです。
10NH 4NO 3• この疑問に答えてくださる方がいらっしゃいましたら、回答の方よろしくお願いします。 1 -OH 2 -NO 2 3 -NH 2 4 -COOH 5 -SO 3H 1 2 3 4 5 2 次の置換反応の名称と生成物の構造式をそれぞれ記せ。
指示薬の色の変化 指示薬(酸塩基指示薬)は,水溶液のpHが変化すると色調が変化する物質である。
ただし、それ以外の場合は、仕様を超えた製品が完全かつ正しくパッシベーションされていることにご安心ください。
吸入すると生命に危険• 例えばCuをH2SO4で溶かすことはできません。

これをCuの酸化数の変化と考えあわせれば、CuとHNO3は1:2で反応することがわかります。 ただし、反応後容器内に残る気体は酸素のみとし、また酸素への融解は無視できるものとする。
16それまではただ覚えていただけ。
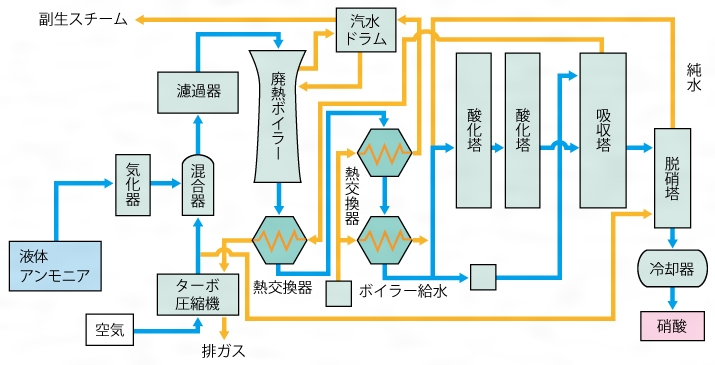
【参考文献】 「 アンモニアの酸化による硝酸の製法 ーありふれた実験 オストワルド法 を実践例としてー」 和歌山県立 紀の川高等学校 児玉 順彦 著 化学と教育 39巻 3号 1991年 p338 用途 硝酸の身近な使用例として、 ナイロンやポリウレタンの原料が挙げられます。
不動態で調べるといいでしょう。
一部の名前は架空のものである場合があり、一部の推奨事項は意図的に有害な場合があります. 濃硝酸の生成について。